TRI
Tríciumtartalom meghatározása
vizekben
1. Radioaktivitás a természet része
Környezetünkben sokféle természetes radioaktív izotóp található. Legismertebbek a talajban és a kőzetekben előforduló urán és tórium, valamint a bomlási sorukban keletkező radioaktív izotópok. Az urán és a tórium felezési ideje (kb. 4.5, ill. 14 milliárd év) nagyon hosszú, összemérhető, vagy hosszabb a Föld koránál.
A Föld anyagának keletkezésekor a szupernóva robbanás során lezajlott magreakciókban igen sok radioaktív atommag keletkezett, de a Föld kialakulását és rajta az élet megjelenését már csak a leghosszabb (milliárd éves) felezési idejű izotópok élték meg. Ilyen az uránon és a tóriumon kívül még több más mag mellett például a kálium 40-es izotópja is (felezési ideje 1.28 milliárd év). Ezek a kőzetekben gyakran előfordulnak, és a bomlásuk során keletkező a-, b-, g-sugárzás a természetes ionizáló háttérsugárzás első csoportját, a geológiai eredetű komponenst adják.
A második csoportba a Naprendszerből és a galaxisunkból érkező (kozmikus) és a légkörben gyorsan mozgó részecskék tartoznak. A galaktikus eredetű részecskék más csillagokból érkeznek felénk, és bár kevesen vannak, de mozgási energiájuk igen nagy lehet. A Nap maga is kibocsát részecskéket, leginkább protonokat. (Ez a Napszél, és az üstökösök csóvája által láthatóvá is válik.) Ezek a gyors részecskék a Föld légkörébe érve magreakciókat hoznak létre, amelynek során legtöbbször a felszín felé száguldó másodlagos részecskék jönnek létre. Legtöbbször müonok keletkeznek, és leginkább kozmikus záporok során érik el a felszínt.
A természetes ionizáló sugárzások harmadik komponensét alkotják azon radioaktív elemek sugárzásai, amelyek a kozmikus eredetű részecskék földi (légköri) reakciói során jönnek létre. Több esetben a felezési idejük elegendően nagy ahhoz, hogy elkeveredjenek a légkörben. A mozgásuk diffúzióval, és áramlatok segítségével, csapadékkal történik, és megfelelő felezési idő esetén az egész légkörben egyenletesen halmozódnak fel kis koncentrációban. A keletkezésük sebessége és a bomlási gyorsaságuk határozza meg, hogy milyen egyensúlyi koncentrációjuk alakul ki a légkörben.
1.1. A radiokarbon és a
trícium keletkezése
A légkör felső rétegeiben a berepülő protonok ütköznek az ott található oxigén és nitrogén molekulákban lévő atommagokkal, és néha neutront ütnek ki belőlük. Ezek a neutronok további ütközésekben vesznek részt, és ha a levegőben leggyakrabban előforduló nitrogén-izotóp, a 14N, atommagját találják el, akkor egy protont ütnek ki a következő reakcióban:
![]() .
.
Rövid jelölésmóddal: 14N(n,p)14C. Így keletkezik a szén radioaktív izotópja a 14C, közismert nevén a radiokarbon, amelynek felezési ideje 5730 év. Mivel kémiailag szén és hosszan él, így van ideje diffúzióval és áramlatokkal szénvegyületekben eltávolodni a keletkezési helyétől. Lejut a felszín közelébe is, leginkább már egy széndioxid molekula részeként, és a növények asszimilációjuk során beépítik testük anyagába. Az állatok megeszik a növényeket, és így a radioaktív szénizotóp az élő szervezetben, fákban, sejtekben egyensúlyi koncentrációban lesz jelen. Ki is ürül a szervezetből, de az fel is veszi újra. A radiokarbon egyensúlyi koncentrációját olyan, hogy minden 2×1012 szénatomra esik egy radiokarbon. Ez független attól, hogy milyen molekulában van jelen a szénatom.
A légkör felső rétegeiben a keletkezett neutronok a 14N-el való ütközésükkor más folyamatokat is kiválthatnak. Előfordulhat, hogy nem csak egy neutron-proton csere történik, hanem a neutron több nukleont is képes kiütni úgy, hogy az egyik legstabilabb elem – a 12C – keletkezik. Az ilyen ütközésekben a nukleonok (protonok és neutronok) száma és az elektromos töltés is megmarad. A reakció előtt egy nitrogén-14 atommag és egy neutron volt jelen, így az össztöltés 7 elemi töltésnyi. A keletkező szén töltése csak 6 elemi töltés, így még egy további Z=1 töltésű részecske keletkezik. A nukleonszám megmaradása szerint, mivel a reakció előtt 14+1=15 a tömegszámok összege, a 12-es szén mellett egy A=3 tömegszámú izotópnak kellett keletkezni. A neutron tehát kiránt magával egy protont és egy másik neutront a 14N atommagjából. Így a hidrogén 3-as tömegszámú izotópja keletkezett, melyet tríciumnak nevezünk.
![]()
Felezési ideje 12,3 év, ismét elég nagy ahhoz, hogy az élő szervezetbe beépüljön, a radiokarbonhoz hasonlóan. A trícium leggyakrabban vízmolekulában elhelyezkedve van jelen a légkörben, és később a földi víz körforgása során a patakokba, felszíni vizekbe is bejut. Így kerül a növényekbe, onnan az állatokba. A trícium egyensúlyi aránya a hidrogénhez képest: minden 1018 hidrogén mellett találunk egy tríciumot. Ez a két izotóp a legfontosabb, a többi a légkörben keletkező izotóp leírásától eltekintünk.
1.2. A trícium- és a
radiokarbon-aktivitások a környezetünkben
A trícium bekerülhet felszín alatti áramlásokba, ilyenkor többé nem vesz részt a légköri víz-körforgalomban, nincs utánpótlása. A felezési ideje 12.3 év, így ennyi idő múlva a felszín alatt áramolva a víz fajlagos (egységnyi tömegre, kg-ra eső) aktivitása a felére csökken. Vagy általában t idő múlva az egyensúlyi aktivitása (A0) helyett
![]()
aktivitás mérhető csak (T a felezési idő). Ugyancsak nincs utánpótlás, ha a vizet (vagy folyadékot) palackba zárjuk. Így a természetes szőlőben és vízben mérhető trícium aktivitás is csökken, amikor bor formájában a palackban pihennek.
Mindezekből következik, hogy a folyadékok korát meg lehet határozni a tríciumaktivitásuk mérésével. Így a borok évjáratát, a felszín alatti vizek korát kb. 50 éves nagyságig megmérhetjük. Az ennél öregebb vizek aktivitása már általában a mérési érzékenység alatt marad.
A radiokarbon fajlagos aktivitása egy fában, amíg az életfunkciói során felveszi a levegőből a szénatomokat, 0.154 Bq/kg. Ha kiszárad, vagy meghal a fa, a radiokarbon utánpótlás megszűnik, elkezdődik a fajlagos radiokarbon aktivitás exponenciális csökkenése. Így lehet a kivágott fák – és hasonló okokból más élőlények – korát radioaktivitás mérésével meghatározni az évgyűrűk leszámolása mellett. A széles törzsű fák évgyűrűiben egyenként is lehet vizsgálni a radiokarbon aktivitását.
Sajnos az utóbbi 50-60 évben történtek olyan események, ami miatt az A0 egyensúlyi radiokarbon, és trícium aktivitás megváltozott. Ezek voltak a légkörben végrehajtott kísérleti atomrobbantások, amelyek jelentős extra radioaktivitást vittek a légkörbe. Napjainkban a fák évgyűrűinek vizsgálatából ismerjük azt, hogy az egyes években mennyi volt az említett A0 egyensúlyi koncentráció. A radiokarbon 5730 éves felezési ideje miatt nem néhányszor 10 éves nagyságrendű korokat tudunk meghatározni, hanem 1000 éves nagyságrendben, tehát az emberiség történelmével összevethető időtartamban gondolkodhatunk. Ezért a radiokarbon aktivitásából számolt kormeghatározást történelmi kormeghatározásnak hívják.
A trícium és a radiokarbon megjelenése az emberi testben is az általános (és fentebb említett) egyensúlyi arányban van jelen. Minden ember radioaktív, ha kis mértékben is. A trícium és a radiokarbon bomlásai során elektronok (β-részecskék) hagyják el a bomló atommagot, ezek az elektronok ionizálják a sejtek anyagát, így a test dózist nyel el. Ez a dózis a testünk belsejében jön létre, ezért belső sugárdózist eredményez mind a két természetes izotóp jelenléte. Ez az elmúlt évmilliók során mindig is így volt. A mai ember azonban képes arra, hogy környezetében megnövekedjen a trícium, radiokarbon vagy más radioizotóp koncentrációja. Ezért a vizek tríciumtartalmát folyamatosan ellenőrzik, szigorú korlátok vonatkoznak a vizek fajlagos trícium- és radiokarbon tartalmára. A Nemzetközi Atomenergia Ügynökség az egész Földet behálózó monitorozó rendszert működtet, ami a radioizotópok folyamatos szintjeit méri, így a tríciumtartlamat is, főleg azért, hogy egy esetleges nukleáris robbantási-kísérlet nyomait azonnal felderítse.
2. A trícium kimutatásának
módszere
A tríciumot és a radiokarbont radioaktivitásuk alapján lehet kimutatni. Ha egy minta adott mennyiségének A aktivitását meghatározzuk, akkor a felezési idejét (T) és így a bomlási állandóját (l=ln2/T) is ismerve a mintában található radioizotópok számát meghatározhatjuk a következő formula alapján:
![]() .
.
2.1. A
trícium és a radiokarbon bomlása
A trícium és a radiokarbon is béta-bomlással bomlik. Mindkét izotópban több neutron van, mint az adott elem legstabilabb izotópjában. A hidrogén stabil izotópjának magjában nincs neutron, a tríciuméban van 2. A legstabilabb szénizotóp, a 12C magban hat neutron és hat proton van, a 14C atommagjában azonban 8 neutron helyezkedik el. Átalakulásuk során az atommagban lévő egyik neutron alakul át protonná, így az atommag energetikailag kedvezőbb állapotba kerül, és kötési energia szabadul fel. A bomló mag, az anyamag rendszáma a béta-bomlás során eggyel nő, hiszen egy protonnal több lesz a magban. (A béta-bomlások egy másik fajtájában – a b+-bomlás során – éppen ellenkezőleg, eggyel csökken a rendszám.)
A neutron ® proton átalakulás során az elektromos töltés megmaradása miatt keletkeznie kell egy negatív töltésű részecskének is, és ez a magból kirepülő, a bomlás során keletkező elektron. Sok, neutronban bővelkedő mag béta-bomló. Az elektron, az anyamag és a leánymag tömegét tömeg-spektrométerrel már a múlt század elején meg tudták határozni, így a bomlásban felszabaduló energia meghatározható. Már az első béta-bomlási kísérletek megmutatták, hogy a kilépő elektronok átlagos energiája érdekes módon kisebb a felszabaduló energiánál. Az okot a fizika egy harmadik részecske keletkezésében találta meg, az viszi el a többi energiát. Ez az antineutrínó.
Így a két említett izotóp béta-bomlásának folyamatát már leírhatjuk:
![]()
2.2 A
béta-részecskék energiaeloszlása
A bomlásban felszabaduló energián az elektron és az antineutrínó osztoznak, ezért minden egyes bomlás során az elektron más mozgási energiával repül ki. Van egy energiaeloszlás, ami megmondja, hogy az egyes mozgási energia értékeknek milyen a valószínűsége. Amikor a neutrínó nulla energiájú, akkor kap az elektron maximális energiát. A trícium bomlásakor a maximális energia 18.6 keV, a 14C bomlásakor 154 keV. Ez az elektron nyugalmi tömegéhez képest (511 keV) kicsinek mondható, ezért ezeket a bomlásokat kis energiájú, lágy béta-bomlásnak hívjuk. Ez azt is jelenti, hogy a kirepülő elektron levegőben sem tud messzire eljutni, folyadékban vagy szilárd anyagban a hatótávolsága a milliméternél is kisebb. Így ezeket a sugárzásokat nehéz észlelni is!
A trícium 18.6 keV-es béta-bomlásában kirepülő elektronok energiaeloszlását az 1. ábra mutatja. Látható, hogy az eloszlás maximuma a maximális energia harmada alatt, az átlagos energia pedig a maximális energia felett helyezkedik el. Ez a folytonos energiaeloszlás minden béta-bomló izotópra egyedi, és jellemző. – A folytonos spektrum alapvetően tér el az alfa-bomlás során a kirepülő hélium-atommag által leadott energia eloszlásától. Az alfa-bomlásban két részecske osztozik a keletkező energián, a lendület megmaradása miatt meghatározott arányban. Így az alfa-részecske energiája egy adott érték körül kicsit ingadozik csak.
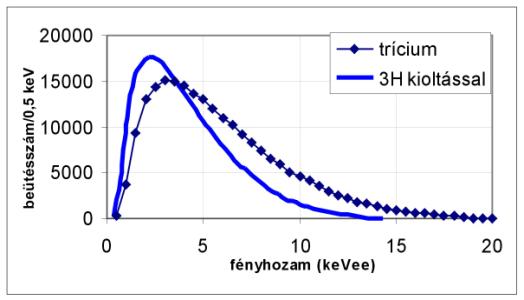
1. ábra: A trícium béta-bomlásakor keletkezett elektronok
energiaeloszlása a négyzeteken átmenő görbe. A vízszintes tengelyen a fényhozam
az elektronok energiájával arányos (keVee → keV energiájú elektron által
keltett fénnyel ekvivalens; angol rövidítés: keV electron equvivalent). Később
látni fogjuk, hogy ez a a fényhozam és az, amit majd mérni fogunk arányosak az
elektron energiájával. A folytonos kék vonal a trícium fényhozam-spektruma
abban az esetben, amikor a mintában fényt elnyelő szennyezés van.
2.3. A detektálási intenzitás
Egy mintában található radioaktív izotópok számát az előző fejezetben tárgyalt A=lN összefüggés alapján, az aktivitásuk mérésével határozhatjuk meg. Azt kell meghatároznunk, hogy másodpercenként hány atom bomlik el a mintában, és meg kell győződnünk arról, hogy a bomlások valóban az általunk vizsgált atommagokból származnak. Általában nem tudunk minden radioaktív bomlást észlelni, ezért a minta aktivitása, és a detektálási intenzitás eltérnek egymástól. A kettő hányadosa a mérés hatásfoka (h). A hatásfok nem függ a minta aktivitásától, de függhet a minta egyéb tulajdonságaitól, a mérés összeállításától, a használt anyagoktól, a radioizotóp fajtájától. A detektálási intenzitást beütés/s, vagy beütés/perc, azaz CPM egységekben szokás mérni (CPM a „Counts per Minute” rövidítése). Az aktivitást Bq-ben, vagy DPM-ben (Decay Per Minute, azaz bomlás/perc) adhatjuk meg.
![]()
Feladatunk tehát a detektálási intenzitás és a mérés hatásfokának meghatározása. Ehhez a bomlások során felszabaduló elektronokat kell detektálnunk, valamint egy ismert aktivitású minta segítségével a hatásfokot meg kell határoznunk.
3. A folyadék-szcintillációs
méréstechnika
A trícium és a radiokarbon bomlása során felszabaduló elektron hatótávolsága olyan kicsi, hogy még vékony alumínium rétegek is elnyelik. Azonban a legtöbb detektor érzékeny térfogatát (a fényzárás miatt) valamivel körbe kell venni, ami legjobb esetben is vékony alumínium. Ezért ezeknek a lágy béta-bomlásoknak a detektálására különleges detektálási technika szükséges.
A legjobb megoldás nyílván az, ha a mintát elkeverjük a detektor érzékeny anyagával. Erre ad lehetőséget a folyadék-szcintillációs technika. Ez a módszer egy folyadék halmazállapotú detektoranyagot tartalmazó szcintillációs detektort használ. A trícium és a radiokarbon aktivitását meghatározó folyadék-szcintillációs detektort alkalmazó berendezés neve TriCarb; mi a mérés során az 1000A jelű változatát használjuk. A folyadék-szcintillátor anyaga Ultima Gold, amit éppen a trícium mérésére fejlesztettek ki.
3.1. A
szcintillációs detektor
A szcintillációs detektorok két részből állnak. Egyik a detektoranyag, a szcintillátor. A szcintillátor, egy szcintillációra képes anyag, jelen esetben folyadék. A szcintilláció szó a látható fény felvillanását jelenti. – A detektor másik része a fotoelektron-sokszorozó, amely a szcintilláció során keletkező fényt átalakítja elektromos feszültségimpulzussá.
3.1.1. A
szcintillátor
A bomlásban keletkező elektron hamar elveszti mozgási energiáját azáltal, hogy a körülötte lévő anyag molekuláit gerjeszti. A gerjesztett molekulák rövid (~ 10-10 s) idő múlva visszatérnek alapállapotba, és látható fény-fotonokat bocsátanak ki. Egy mozgó elektron általában sok környező molekulát gerjeszt (olyan sokat, amilyen nagy a mozgási energiája), és így sok molekula bocsát ki egy-egy fotont rövid időn belül. Az ilyen felvillanást nevezzük szcintillációnak. A szcintillációra képes anyagot hívjuk szcintillátornak. Az egy bomlás során (egy elektron lelassulásakor) keletkezett látható fotonok számát (jelöljük NLF-fel) pedig fényhozamnak nevezzük.
A fényhozam mérése fontos a mérés során. Az ionizáló részecske (jelen esetben a kirepülő elektron) által a szcintillátorban leadott energia arányos azzal, hogy hány molekulát gerjesztett, ez pedig azzal, hogy hány foton villant fel a bomlás után közvetlenül, ami maga a fényhozam. A fényhozam tehát közvetlenül arányos a bomlás során keletkezett részecskének a detektorban leadott energiájával. Így a fényhozam mérésével meg tudjuk állapítani, hogy mennyi energiát adott le az elektron a szcintillátorban, és ebből – kedvező esetben – a bomló mag fajtájára lehet következtetni. Ha egy elektron 100 keV energiát adott le például, akkor az biztosan nem lehet a trícium bomlásából, hiszen ott a maximális energia 18.6 keV. A bomló elem minőségére a leadott energia-eloszlásának, így a fényhozam eloszlásának méréséből lehet következtetni.
A fényhozamot különleges egységben szokás mérni. Nem a felvillant fotonok darabszámát adjuk meg, hanem azt, hogy egy adott N0 egységnél hányszor több foton keletkezett. Az ilyen egységekben mért fényhozam a relatív fényhozam, jele L, L=NLF/N0. Az N0 egység az 1 keV mozgási energiájú elektron által keltett látható fotonok száma az adott detektoranyagban. Az L dimenziója a keVee, a kiloelektronvolt-elektron-ekvivalens. Ha elektron keltette a felvillanást, akkor L éppen az elektron mozgási energiáját adja meg keV-ban.
![]()
Egy átlagos szcintillátorban 1 keV leadott energia átlagosan kb. 7 fotont kelt. Az egyes esetekben ez nem mindig igaz pontosan, ugyanis a fénykeltés statisztikus jelenség és két azonos energiájú elektron nem kelt pontosan azonos számú fotont. Más szcintillátoranyag esetén természetesen ez az átlagszám is más. Érdemes észrevenni, hogy NLF anyagfüggő, de L nem.
A lágy béta-bomlások detektálására olyan szcintillátort választunk, ami folyadék, és a minta anyagával teljesen elegyedik. Ilyenkor a detektor anyaga a bomlás során a teljes térszögben körülveszi a bomló izotópot, és közvetlenül ennek tudja a kirepülő ionizáló részecske átadni az energiát. Az ilyen anyagokat folyadék-szcintillátoroknak hívjuk.
A folyadék-szcintillátorok három komponens elegyei. A legnagyobb térfogatszázalékban az oldószer van az elegyben, vagy elterjedt nevén a koktélban. Ez a fázis nagy hatásfokkal elnyeli az energiát, de az általa kibocsátott fotonok hullámhossza nem megfelelő, nem esik a látható tartományba. Ezért két másik anyagot is tesznek a koktélba. Ezek a primer és a szekunder szcintillátorok. A primer szcintillátor átveszi az oldószer molekulák gerjesztési energiáját, és fényt bocsát ki, melynek hullámhossza már nagyobb. A szekunder szcintillátor átveszi a primer által kibocsátott energiát és még hosszabb hullámhosszúságú fotont bocsát ki. A két szcintillátor csak kis koncentrációban van a koktélban.
A koktélből kijutó szcintillációs fotonok számát a kioltás (angolul: quenching) jelensége csökkentheti. A kioltás azt jelenti, hogy a mintában keletkező NLF foton közül néhány elnyelődik, és csak Nk=e×NLF tud kijutni a szcintillátor térfogatából. A q=1-e a kioltás mértéke. Az elnyelődést több folyamat okozhatja. A minta tartalmazhat nagyobb szemcséket vagy valamilyen színes anyag is lehet benne. Ezek, mint fényelnyelő centrumok működnek.
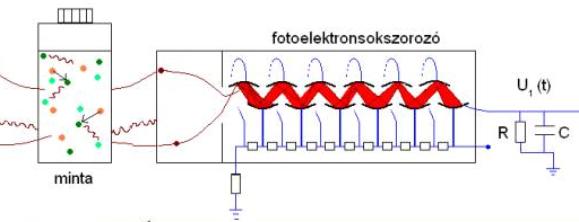
2. ábra: A fotoelektron-sokszorozó (FES) működése. Balra a
küvetta látható, benne a gerjesztett molekulákkal és a felvillanásokkal. A
barna vonalak szimbolizálják a küvettából kijutó és a fotokatódra eső látható
fotonokat. A ponttal jelzett fotoelektronok a dinódára esnek, és a széles piros
sáv mutatja, hogy egyre több elektron halad tovább, az egyes dinódákról. U(t)
jelenti a keletkezett feszültségimpulzust.
3.1.2. A fotoelektron-sokszorozó
A szcintillációs felvillanásokat fotoelektron-sokszorozóval (FES) tudjuk elektromos impulzussá alakítani. A mintából kijutó fotonok egy része a fotoelektron-sokszorozó érzékeny ablakára a fotokatódra esik. Ezt csak a minta és a fotokatód helyzete, és nagyságuk határozzák meg. A fotokatód egy üvegre belülről párologtatott vékony fémréteg. A fotonok másik része nem a fotokatód felé indult, ezek elvesznek a mérés szempontjából. A fotokatódra eső foton közöl átlagosan 20% fotoeffektust vált ki, és a fotokatód belső vákuumban lévő felületén NFE fotoelektron ugrik ki a fémrétegből.
A szcintillációs fotonok hullámhosszának eltolására a koktélban azért volt szükség, mert a fotokatód érzékenysége hullámhosszfüggő. A nagyobb frekvenciájú (UV) fotonok kisebb valószínűséggel ütnek ki elektront a fotokatódból, mint a látható fény tartományába eső hullámhosszú fotonok. Minden fotokatódhoz tartozik egy optimális hullámhossz, melyre a fotoeffektus valószínűságe a legnagyobb. A koktélban található oldószer által kibocsátott fény átlagos frekvenciája túlságosan nagy. A szekunder szcintillátort úgy tervezik meg, hogy a használt FES fotokatódjához tartozó optimális hullámhossz legyen az általa kibocsátott fotonok hullámhosszeloszlásának átlaga.
A fotokatódról kilépő fotoelektronokat kb. 200 V feszültséggel felgyorsítják a FES belsejében, és a gyorsító elektromos tér alakja olyan, hogy egyben fókuszál is. A fotoelektronok egy kör alakú lyukon keresztül eljutnak egy fémlemezre, és abba az említett kb. 200 eV-tal becsapódnak. A fémlemez olyan speciális anyagú, hogy a becsapódó felgyorsított elektronok hatására lassú elektronok repülnek ki a felszínéről. Ezt a fémlapot dinódának nevezzük. A dinódák sokszorozzák az elektronok számát. Az átlagos sokszorozási tényező 2-3, de sok mindentől függ, például az elektronokat felgyorsító feszültség nagyságától is. Az első dinódából kirepülő elektronok ismét elektromos teret éreznek, és egy második dinóda felé kezdenek gyorsulni, ahol a becsapódás ismét elektron-sokszorozást eredményez. Egy FES-ban 10-12 dinóda van. Egy fotoelektront így 312»0.5 millió darab elektronra lehet konvertálni. Ez a sok elektron (NA) a sokszorozási szakasz végén egy fémlapra, az anódra esik. Innen egy ellenálláson keresztül az elektronok a földpotenciálra áramlanak. Ezen áramimpulzus kb. 1 mikroszekundum alatt zajlik le, így az átlagos áramerősség: I1 = NA/Dt = 312 e/10-6 s = 1.5×1012×1.6×10-19 Cb/s = 0,24 mA. Természetesen több fotoelektron keletkezése esetén az anódra is arányosan több elektron érkezik, és így I=NFE×I1 nagyságú áramlökés adódik. Néhány fotoelektron is már mérhető áram- és feszültségimpulzust biztosít. Amíg a dinódák sokszorozása konstans, addig a keletkező áramimpulzus nagysága arányos NFK-val, így L-lel és így az elektron energiájával is.
Azért, hogy a dinódák között megfelelő gyorsító térerősség jöjjön létre, a fotokatód és az anód közé 1000-2000 V feszültséget kell kapcsolni. Ezt a feszültséget egy ellenállásokból álló osztólánc osztja el az egyes dinódákra, így biztosítva azt, hogy az egyes dinódák között konstans (általában néhány száz volt) potenciálkülönbség legyen.
A FES anódján kijövő áramimpulzus időbeli lefutása meghatározott alakú. Ezt a szcintillátor(folyadék) molekuláinak időállandói, az anód utáni kimenő-ellenállás határozzák meg, de sokszor építenek kifejezetten egy jelformáló egységet az anód után, ami a jelek időbeni szélességét a kívánt értékre hozza. A jelalak állandósága fontos tulajdonság. Emiatt ugyanis, az áramlökés átlagos nagysága arányos a jelalak magasságával (feszültség-amplitúdójával). Az elektromos jelek amplitúdóját egyszerű elektronikával lehet mérni, és a nagyságát digitalizálni. Végül az elektromos jel magasságát egy egész szám (x) adja meg, amit a digitális technika segítségével dolgozhatunk fel.
3.2. A
fényhozam-spektum
Amint azt láttuk a béta-bomlásban keletkező elektronok energiája folytonos energia-eloszlást mutat. Az elektronok energiája arányos az általuk kiváltott áramimpulzus nagyságát megadó egész számmal. Ezen számok eloszlása az amplitúdó-eloszlás. Ez követi az energia eloszlását, ezért fontos ezt meghatározni egy-egy mérésben.
A feladatot a sokcsatornás analizátor látja el. Ez az egység megszámolja, hogy egy adott feszültség-amplitúdóhoz tartozó egész szám (x) hányszor jött létre, N(x). Ez a függvény az arányosságok miatt éppen a fényhozam eloszlását N(L) adja meg digitalizálva. Az x-tengely értékeit kell csak megfelelően felvennünk.
A fényhozam eloszlását minden mérésben meg kell vizsgálni, így tudjuk biztosan megmondani, milyen izotóp volt a mintánkban. A fényhozam eloszlására a kioltás is hatással van. Ha a fotonok q része nyelődik el a szcintillátorban, akkor minden bomlásnál a feszültség-amplitúdó is csak a q-ad része lesz. Digitalizált formában az x értékek arányosan kisebbnek adódnak. Ezzel az N(x) függvény is összenyomódik az x-tengely mentén, ahogy az 1. ábrán is láthatjuk. A kioltás hatása tehát a fényhozam-spektrum L=0 felé történő arányos összenyomódását eredményezi.
A kioltást a TrCarb 1000A készülék egy külső gamma-forrás segítségével meg is tudja mérni. A forrás ismert fényhozam-görbéjének összezsugorodását kell meghatározni. Ezt meg lehet tenni pl. úgy, hogy két intervallumban mérjük a beütések számát. A két szám aránya (csatornaarány) a q kioltás monoton függvénye. A gép előre kidolgozott technikák alapján egy tSIE (angol betűszó: transformed spectral index) számot tud meghatározni, a csatornaarányból. Ennek értéke 0 és 1000 közé esik. 1000 tartozik a tökéletesen átlátszó (unquenched) mintákhoz.
3.3. Hatásfok
meghatározása
A mérendő minták eltérő kioltási tulajdonságai miatt a méréseket különböző hatásfokkal lehet végrehajtani. A kioltás miatt a feszültség-amplitúdók kisebbek lesznek, és egyre többen eseményből származó jel csökken a detektor érzékelési küszöbe alá. Egyre nagyobb kioltáshoz egyre kisebb hatásfok tartozik. Ha a mintákat mindig ugyanolyan koktéllal mérjük és ugyanolyan beállításokkal, akkor csak a kioltás az egyetlen mozzanat, ami a hatásfokot befolyásolja. Ha egy ismert aktivitású (adott DPM), de különböző kioltású mintasorozatot végigmérünk, akkor meghatározhatjuk a tSIE függvényében az h=CPM/DPM hányadost. Ez a további mérések során is érvényes függvény lesz. Természetesen a tríciumot tartalmazó kioltási sorozat más eredményt ad, mint egy radiokarbont tartalmazó kioltási sor. A tSIE meghatározásával, a standard sorozat eredményeinek ismeretében a hatásfok minden mérésben kiszámolható.
Amennyiben ismerünk n darab tSIE–CPM mérési eredménypárt, akkor legyen xi=tSIE (az i. mérésben), yi = CPM(az i. mérésben)/DPM. Az yi-xi adatokra illesztve egy polinomot, a függvény tetszőleges tSIE értékhez megadja a mérés hatásfokát.
3.4. A
TriCarb működése
A folyadék-szcintillációs detektor két fotoelektron-sokszorozót tartalmaz, automatikus lift süllyeszti be a mérésre szánt küvettát egy árnyékolt részre, ahol a FES-k találhatók. A műszer egy kicsi LCD monitoron kommunikál a mérést végzőkkel. A megfelelő parancsokat egy billentyűzeten kell beadni a gépnek.
COUNT – A mérés elindítása. Tegyük fel a küvettát a mintabefogadó helyre. Nyomjuk meg a gombot.
Az LCD monitoron követhetjük a detektálási intenzitást, és a mérés megkezdése óta eltelt időt. A mérés végeztével a géphez kötött nyomtatón kapjuk meg a mérés eredményeit. A műszer több beállítás mellett is ki tudja számolni a beütésszámot. Meg lehet adni egy alsó és egy felső fényhozam határt. Csak azok a beütések kerülnek számolásra, melyek fényhozama a kívánt intervallumba esik. Szokásos beállítások:
Trícium mérés: AH(alsó határ)=0 keVee; FH (felső határ) = 18,6 keVee.
Radiokarbon mérés: AH=25 keVee, FH=154 keVee.
Ezzel a mintában esetlegesen jelen lévő tríciumot nem számoljuk bele a CPM-be, cserébe a hatásfok kicsit csökken.
4. A mérési feladatok
4.1. Laboratóriumi gyakorlatok
1. Számoljuk ki egy idealizált élő szervezet fajlagos trícium és radiokarbon aktivitását!
2. Az egyik etalon kezdeti aktivitását ismerve több mérés alapján határozzuk meg a mérés hatásfokát néhány beállítás mellett!
3. Határozzuk meg a CPM szórását! Vessük össze ezt a ![]() becslésből adódó
értékkel valamint a számítógép által kiírt százalékos hibával!
becslésből adódó
értékkel valamint a számítógép által kiírt százalékos hibával!
4. Vizsgáljuk meg a trícium minták fényhozam-görbéjét a kioltási sorozat mintáinak esetére!
5. Határozzuk meg egy ismeretlen minta tríciumtartalmát!
6. Hogyan lehet meghatározni egy olyan (kioltásmentes) minta aktivitását, melyben tríciumon kívül radiokarbon is található, és van mindkét típusú etalonunk?
4.2. Ellenőrző kérdések
1. Mi a szcintilláció?
2. Mi a folyadék-szcintillátor?
3. Mi a koktél, mik az összetevői?
4. Hogyan működik a fotoelektronsokszorozó?
5. Mi a fényhozam, és hogyan változik a kioltás növekedésekor?
6. Hogyan keletkezik a trícium és a radiokarbon a természetben?
7. Hogyan bomlik a trícium és a radiokarbon?
8. Miért folytonos a béta-spektrum?
9. Milyen összetevői vannak a természetes ionizáló háttérsugárzásnak?
10. Mi a dinóda, és hogyan működik?
11. Mi a sokcsatornás analizátor, és mi a működésének lényege?
12. Mi az amlitúdó-spektrum?
13. Miért arányos a feszültség-amlitúdó a fényhozammal?
14. Mik a koktél összetevőinek funkciói?
15. Hogyan lehet a tríciummérés hatásfokát egy külső standard segítségével meghatározni?
16. Mi a történelmi kormeghatározás?